基因敲入细胞定制
基因敲入细胞定制 技术简介 利用CRISPR/Cas9技术,针对靶基因设计,构建相应的Cas9/sgRNA和Donor质粒,将Cas9/sgRNA和Donor质粒共转染目的细胞,通过sgRNA引导Cas9核酸酶对
基因敲入细胞定制
技术简介
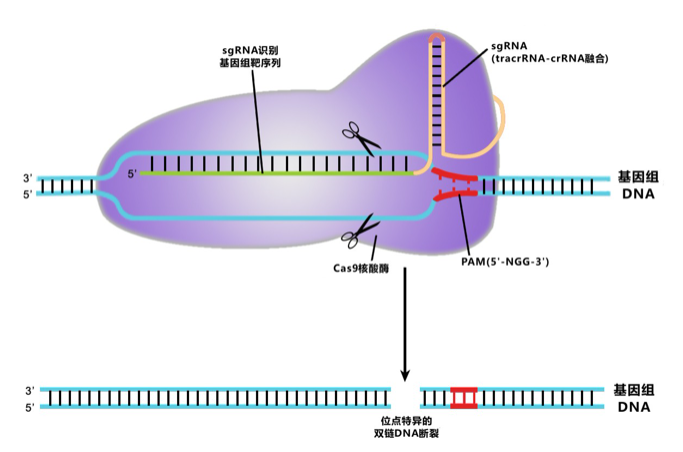
利用CRISPR/Cas9技术,针对靶基因设计,构建相应的Cas9/sgRNA和Donor质粒,将Cas9/sgRNA和Donor质粒共转染目的细胞,通过sgRNA引导Cas9核酸酶对目的基因靶位点进行切割,引起DNA双链断裂(Double-strand breaks DSB),通过细胞自身的同源重组修复(Homology -directed repair HDR)途径,将Donor中的外源基因定点敲入到目的细胞的基因组中。
![]()
应用范围
| 1 | 2 |
| 可在指定基因位点敲入外源目的基因,避免因随机整合带来的多位点插入,表达不稳定,基因破坏等问题 | 通过该方法可在内源基因N或C端定点引入外源报告基因,实现内源基因的示踪。 |
方案选择
| 1 | 2 |
| 拥有多种荧光筛选标记,结合流式分选,可提高获得阳性目的细胞概率 | 在细胞不产生耐药的情况下,可提供多种药筛标签,满足不同实验需求 |
应用案例
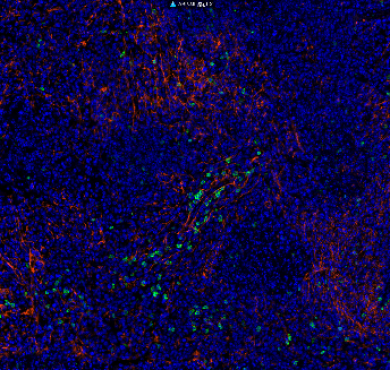
19-28z(CAR)片段敲入TRAC位点目的细胞株的构建(引自:Eyquem J,et al., Nature ,2017)。
利用CRISPR/Cas9技术,用病毒感染目的细胞,将病毒中包含的目的序列(19-28z)整合入TRAC基因组中,19-28z受TRAC内源启动子调控,可以转录翻译成CAR蛋白,同时19-28Z敲入阻断TRAC转录翻译成TCR蛋白。通过流式分选,筛选CAR表达阳性且TCR表达阴性的细胞,得到19-28z(CAR)片段敲入的目的细胞株。


项目流程与周期

交付标准
| 1 | 2 | 3 |
| 按指定方案构建的目的基因编辑细胞株,每个目的细胞株交付基因型正确的2个克隆,每个克隆2支冻存细胞(1*10 cells/支) | 对应野生型对照细胞 | 项目报告及质检报告 |