基因移码敲除
技术简介根据目的基因外显子序列设计并合成sgRNA,将Cas9和sgRNA质粒共转染目的细胞,通过sgRNA引导Cas9核酸酶对目的基因靶位点进行切割,引起DNA双链断裂(Double-strand breaks DSB)
技术简介
根据目的基因外显子序列设计并合成sgRNA,将Cas9和sgRNA质粒共转染目的细胞,通过sgRNA引导Cas9核酸酶对目的基因靶位点进行切割,引起DNA双链断裂(Double-strand breaks DSB),通过细胞自身的非同源末端修复(Non-homologous end joining, NHEJ)途径造成目的基因编码区碱基的随机缺失或插入,若缺失或增加的碱基数为非3倍数,则引起目的基因发生移码突变,进而实现目的基因敲除。
应用范围
| 1 | 2 |
| 可实现大部分编码基因的敲除,尤其是需敲除的目的基因存在重合基因或有邻近基因存在时 | 不适用非编码基因和存在多个转录本的编码基因 |
方案选择
| 1 | 2 | 3 |
| 拥有质粒瞬转和慢病毒感染两种传送方式,可实现大多数细胞系和干细胞的基因编辑 | 拥有多种荧光筛选标记,结合流式分选,可提高获得阳性目的细胞的概率 | 在细胞不产生耐药的情况下,可提供多种药筛标签,满足不同实验需求 |
应用案例
细胞名称:C3H10T1/2
基因名称:Piezo1
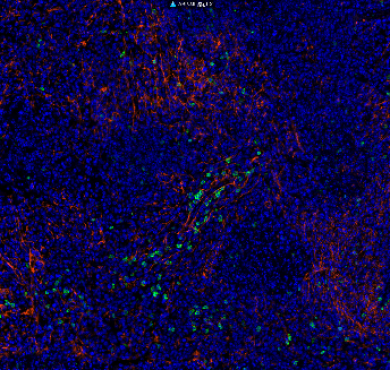
项目方案:构建Cas9和sgRNA过表达慢病毒,感染目的细胞,通过流式分选GFP和mCherry阳性细胞,挑选单克隆,经鉴定后进行扩增,得到Piezo1基因移码敲除的单克隆细胞株。
胞鉴定:通过对流式分选筛选出的单克隆细胞进行PCR及测序鉴定,Piezo1基因第4外显子中产生1个碱基缺失,并在第4外显子中提前形成终止密码子,无法翻译正确蛋白,Piezo1基因在功能上达到敲除的效果。
项目流程与周期
交付标准
| 1 | 2 | 3 |
| 按指定方案构建的目的基因编辑细胞株,每个目的细胞株交付基因型正确的2个克隆,每个克隆2支冻存细胞(1*10ªcells/支) | 对照细胞株,瞬转方案为对应野生型细胞,慢病毒方案为Cas9稳转细胞 | 项目报告及质检报告 |
参考文献